�й������ҽҽҩ�о�����Э�������ĺ���ίԱ��
�칫�ص������Ѿ���Ǩ����������ֱ����С�ֹ�Ӣһ��¥824�ң�
ͬʱΪ��������ϵ���̶��绰�Ѿ����
�º���010��58562339���ش�֪ͨ��
��ַ��������������ֱ����С�ֹ�Ӣһ��¥824��
�ʱࣺ100035
�绰��010-58562339
���棺010-58562339
���䣺cngjzj@163.com
��վ�������ֱַ�����ӡ�����http://www.cngjzj.com/
�����������ֱַ�����ӡ�����http://blog.sina.com.cn/cngjzj
��ͨ·��ͼ ������ۿ���ͼ��
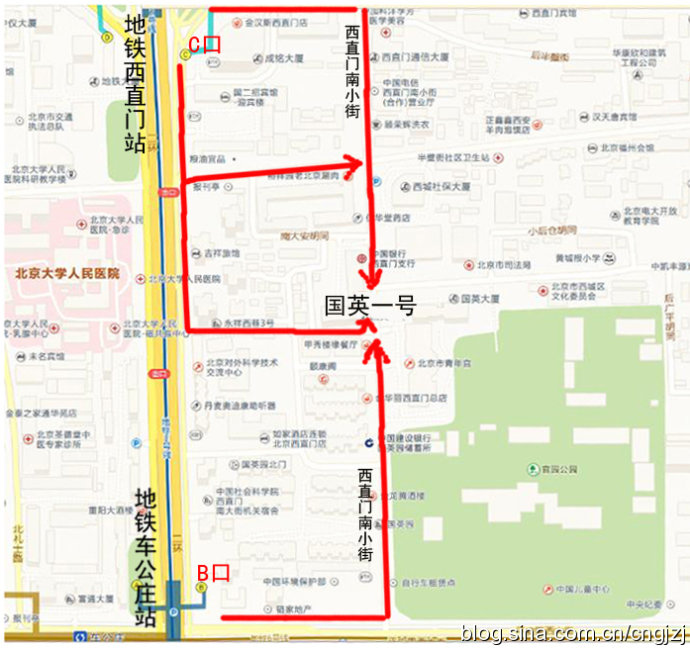
����������������ר�ߣ��ڶ�ֱ��վ�³����˵���2���߿�����ֱ�ŷ�������ֱ��վ C �ڳ�վ��
��������ֱ���ڴ����ֱ��100�ף��ҹյ���ֱ����С�֣����ϲ��е�����·�ڼ�����Ӣ1��¥¥�¡�
2������ֱ��50�ף��ƹ� �����б��� �����д�ͬ����ֱ����С�֣����ϲ��е�����·�ڼ�����Ӣ1��¥¥�¡�
���������ڳ�������ֱ�������Ĵ�ͣ�������վ�³��������������ֱ����С�ֹ�Ӣ1��¥��
������վ��107·����ͨ106·
������ֱ���ϣ�387·��44·��800�ڻ���816·��820�ڻ���845·
��������ׯ������������
������ֱ�ţ�����������
��������ׯ����107·��118·��701·
��������ׯ����209·��375·��392·
2018��10��28��
 ��������
��������
 ��ӡ
��ӡ
 �� �� С
�� �� С
��ʿ��������ҩ�������з��������ε���